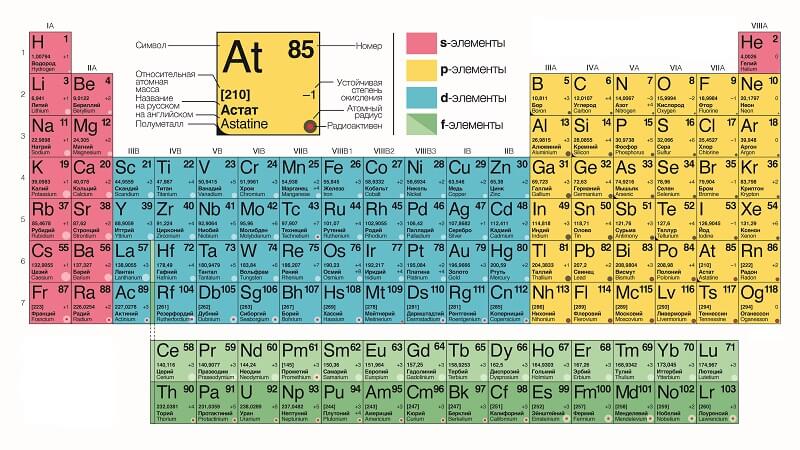
Правила чтения и использования таблицы Менделеева
Из таблицы Менделеева можно почерпнуть огромное количество информации о каждом химическом элементе, что значительно облегчит решение задач. Более того, периодическую систему можно использовать на ЕГЭ, и это может стать серьезным подспорьем. Главное — уметь грамотно ей пользоваться. Как это делать — читайте в нашей статье.
Таблица Менделеева — краткое описание
Таблица Менделеева — это графическое выражение периодического закона, который открыл русский ученый Д.И. Менделеев в 1869 году. Периодическая система представляет собой классификацию химических элементов, которая основана на зависимости свойств химических элементов от заряда их атомного числа. Первоначальный вариант предполагал зависимость свойств веществ от их атомной массы.
Существуют три формата таблицы Менделеева:
- короткий (короткопериодный);
- длинный (длиннопериодный);
- сверхдлинный.
Международным союзом теоретической и прикладной химии (ИЮПАК) в качестве основного утвержден длинный вариант таблицы Менделеева, а короткий вариант официально отменен в 1989 году.
Пустые ячейки в таблице
Создав периодическую таблицу в 1869 году на базе уже известных миру 63-х химических элементов, Менделеев предсказал открытие новых и оставил для них пустые ячейки в таблице. Русский ученый оказался прав. Гипотеза Менделеева в скором времени была подтверждена открытиями других ученых: в 1875 году был открыт галлий, в 1879 — скандий, в 1886 — германий. На 2021 год в таблицу собраны 118 известных элементов. Последние из них открыты в 2016 году: ученые обнаружили нихоний, московий, теннессин и оганесон.
Структура таблицы
В таблице Менделеева химические вещества расположены в специальном порядке: слева направо по мере роста их атомных масс. Все они в периодической системе объединены в периоды и группы. Таблица состоит из семи периодов и восьми групп.
Периоды — это горизонтальные ряды в таблице.
Элементы, которые относятся к одному периоду, показывают следующие закономерности с увеличением их порядкового номера:
- Возрастает электроотрицательность.
- Металлические свойства убывают, неметаллические возрастают.
- Атомный радиус падает.
Периоды в таблице делятся на:
- малые;
- большие.
Малыми называются периоды, которые содержат небольшое количество элементов. Это первый, второй и третий периоды, первый состоит из 2-х, второй и третий из 8 элементов.
Все остальные периоды — это большие периоды. Четвертый и пятый состоят из 18 элементов, шестой — из 32-х, седьмой — из 24-х.
В нижней части таблицы Менделеева расположены химические вещества, которые называются лантаноидами и актиноидами.
Таблица периодической системы содержит десять рядов. Малые периоды состоят из одного ряда, большие периоды содержат по два ряда. В седьмом периоде находится один ряд.
Каждый большой период состоит из четного и нечетного рядов. В четных рядах содержатся металлы, в нечетных рядах — неметаллы.
Периодическая система начинается водородом — первым химическим элементом, а заканчивается на сегодняшний день 118-м — оганесоном. Ученые утверждают, что таблица не закончена, идет активный поиск 119-го элемента.
Группы элементов с похожими свойствами
Группа — это вертикальная колонка в периодической таблице, определяющая основные физико-химические свойства элементов. Вещества, принадлежащие к одной и той же группе, обладают похожими химическими особенностями и демонстрируют одинаковую закономерность в изменении своих свойств по мере увеличения атомного числа.
Всем группам (колонкам таблицы) присваиваются номера от 1 до 18 — слева направо (от щелочных металлов к благородным газам). Такая система вступила в силу в 1988 году по инициативе ИЮПАК. Все прежние названия групп, которые использовали в разных странах, больше не употребляются.
Элементы, которые относятся к одной группе, показывают следующие закономерности по направлению сверху вниз:
- Возрастает радиус атома элементов в рамках одной группы.
- Усиливаются металлические свойства элементов и ослабевают неметаллические.
- Падает электроотрицательность.
Цветовое определение групп
Вещества в каждой группе делятся на те, которые находятся в главной подгруппе и те, которые входят в побочную подгруппу. В таблице составляющие побочной группы выделяются синим цветом, к ней относятся элементы только больших периодов (начинаются с четвертого периода). В главную подгруппу могут входить элементы и малых, и больших периодов (начинаются с первого или второго периодов).
Различение металлов, металлоидов и неметаллов
Все химические элементы в зависимости от их химических и физических свойств можно разделить на 3 типа:
- металлы;
- металлоиды;
- неметаллы.
Характеристика металлов (например, медь, алюминий, золото):
- Хорошая электро- и теплопроводность.
- Способность отражать свет (яркий внешний вид).
- Высокая температура плавления (остаются твердыми при нормальных значениях окружающей среды, исключение — ртуть).
- Пластичность и податливость.
Неметаллы встречаются в природе в трех состояниях: газ (например, водород), жидкость (например, бром) и твердые вещества (например, фосфор). Их характеризуют:
- Неспособность проводить тепло и электричество.
- Разнообразный внешний вид (элементы с низкой плотностью и яркостью).
- Значительно более низкая температура плавления в сравнении с металлами.
- Хрупкость и ломкость.
Металлоиды имеют смешанные свойства металлов и неметаллов (например, кремний). Их основные черты:
- Средняя тепло- и электропроводность.
- Внешний вид может быть схож с металлами или неметаллами.
- Различаются между собой по температуре плавления, плотности, цвету и форме.
Обозначение элементов
Каждый элемент в периодической системе Менделеева имеет несколько обозначений:
- название;
- буквенное выражение;
- атомный номер;
- массовое число.
Буквенное, название
В таблице может быть указано полное название вещества (например, Carbon), в таких случаях его располагают под химическим символом.
Символ — это сокращенное название элемента (например, гелий — He).
Иногда в таблице не указываются названия вещества и приводится лишь его химический символ. Обозначения, как правило, состоят из одной или двух латинских букв. Символ элемента расположен в центре соответствующей ячейки в таблице.
Атомный номер
Атомный номер элемента обычно располагается вверху соответствующей ячейки, посередине или в углу. Все элементы имеют атомные номера от 1 до 118. Атомный номер — это всегда целое число.
Массовое число
Массовое число — это общее количество протонов и нейтронов в ядре. Его легко определить по атомной массе элемента, округляя ее до ближайшего целого числа.
Атомная масса указывается внизу ячейки, под символом элемента. Атомная масса — это сумма масс частиц, которые составляют ядро атома (протоны и нейтроны), представляет собой среднюю величину, для большинства элементов записывается в виде десятичной дроби.
Например, фосфор (P) имеет атомную массу равную 30,97376, следовательно, массовое число (количество протонов и нейтронов в ядре) составит 31.
Валентность
Валентность — это свойство элементов образовывать химические связи.
- постоянная;
- переменная (зависит от состава вещества, в которое входит элемент).
Определить валентность по таблице Менделеева несложно:
- Постоянная валентность идентична номеру группы главной подгруппы. Номера групп в таблице изображаются римскими цифрами.
- Переменная валентность (часто бывает у неметаллов) определяется по формуле: 8 (всего 8 групп в таблице) вычесть № группы, в которой находится вещество.
Например, вещества, находящиеся в первой группе главной подгруппы (Li, К) имеют валентность, равную I; элементы, которые располагаются во второй группе главной подгруппы (Mg, Ca) обладают II валентностью. Мышьяк (As) находится в V группе главной подгруппы, следовательно, значение его валентности также будет равняться V. Помимо этого, у вещества есть еще одно значение валентности. Определяется оно по приведенной выше формуле и равняется III.
Если у вас возникнут сложности в усвоении знаний не только по химии, но и по любому другому предмету, обращайтесь за помощью к образовательному ресурсу Феникс.Хелп. Для нас не существует нелюбимых дисциплин и сложных тем!
Медь как химический элемент таблицы Менделеева
М Медь является химическим элементом с атомным номером 29 и условным обозначением Cu. Медь представляет собой мягкий ковкий пластичный металл с очень хорошей тепло- и электропроводимостью.
Как была открыта медь
Такие металлы как медь, золото, серебро и олово были известны людям очень давно. Так как с медью легко работать, она использовалась древнейшими известными культурами уже 10000 лет назад. Пик популярности использования меди приходится начиная с 5 и заканчивая 3 тысячелетием до Нашей Эры. Это время в некоторых регионах принято называть «медным веком». Из этого металла изготавливались как орудия труда, так и украшения. На территории современного Ирана был найден медный кулон возраст которого приблизительно оценивается в 8700 год до Нашей Эры. Так же медь является первым металлом, который научились легировать с помощью олова и мышьяка до бронзы. В связи с этим открытием, которое произошло вероятно около 3 тысячелетия до Нашей Эры, началась так называемая эпоха «Бронзового века». Эта эпоха продлилась ориентировочно до первого тысячелетия до Нашей эры.
Затем производство меди и его обработка набирала уже значительные обороты. К началу новой эпохи мировое производство меди ориентировочно варьировалось в пределах 15 тонн в год. В первом тысячелетии Нашей Эры уже производились массивные сооружения из меди и его сплавов. В пример можно поставить бронзовую статую Будды храма Нара в Японии. По историческим сведениям ее отлили в 749 году. Для сооружения 16-ти метровой конструкции понадобилось 400 тонн сырья. Научное открытие самого металла можно присудить немецкому ученому Готфриду Осанну. Он изобрел порошковую металлургию, которую использовал на меди в 1830 году. В ходе своих испытаний он описал и определил атомный вес этого химического элемента.
Где и как добывают медь
Как становится понятно из текста выше, такой химический элемент как медь использовался уже с древнейших времен. И добыча этого элемента уже осуществлялась еще до Нашей эры. Медь является третьим металлом по применению после железа и алюминия. Вся добытая медная руда до 1900 года составляет менее 5% от всей руды извлеченной из недр Земли. В 2008 году добыча меди превысила порог в 15 миллионов тонн в год. На сегодняшний день эта цифра готовится превысить отметку в 20 миллионов тонн. Ведущими производителями меди являются Чили, Перу, Китай, США, Конго, Австралия, Замбия, Индонезия, Мексика и Россия.
Процесс получения самой меди выглядит следующим образом. Вначале медный камень Cu2S извлекается из медного гравия CuFeS2. Для этого гравий обжигают с добавлением кокса, а оксиды железа зашлаковывают кремнеземом. Шлак из силиката железа плавает на поверхности и может быть легко слит. Медный камень, оставшийся на дне, затем перерабатывается в черновую медь. Эта процедура обычно осуществляется в два этапа. На первом этапе образовавшийся сульфид железа обжигается до оксида железа и связывается с кварцевым шлаком, который в последующем выливается. На втором этапе две трети медного камня окисляется до оксида. После этого оксид меди реагирует с оставшимся сульфидом в результате чего появляется черновая медь.
Черновая медь имеет чистоту порядка 98%, а оставшиеся 2% приходятся на примеси железа, цинка, серебра и золота. Очистка черновой меди осуществляется методом электролитического рафинирования в серной кислоте. В ходе этой реакции железо и цинк растворяются в виде катионов, а благородные металлы осаждаются на дне. Чистота меди на выходе этого процесса составляет 99,99%.
Распространенность меди
Распространенность такого химического элемента как медь довольно широка. По распространенности в земной коре медь занимает 23 позицию. Ее содержание в земной коре оценивается в 0,006%. Этот химический элемент является одним из немногих, который встречается в природе в самородном виде. Сегодня известно более 3000 мест по всему миру, где ведется добыча меди. Самыми плодородными месторождениями обладают такие страны как Чили, Россия и США. На сегодняшний день, медными рудниками обладают более 50 стран по всему миру.
Так же стоит отметить, что медь по большей своей части добывается в составе минералов, так как в природном виде она встречается довольно редко. На сегодняшний день известно свыше 600 итнералов в составе которых присутствует медь. Самыми ценными из них являются халькопирит, халькозин, борнит, атакамит и малахит. В составе этих минералов процентное содержание меди превышает 60%.
Что же касается распространенности во вселенной, то тут не все так однозначно. Определить его распространенность не представляется возможным из-за малого количества информации. Известно только его присутствие на луне и на марсе по взятым образцам с этих космических тел. Предположительная оценка концентрации не считается маленькой.
Применение меди
Около 98% всей меди используется либо в своем естественном виде, либо в виде сплавов. Широкое применение она находит благодаря своим физическим и химическим свойствам. К основным его своиствам относится пластичность, теплопроводность, электропроводность и устойчивость к коррозии. Для некоторых видов применения медь является слишком мягким металлом, поэтому она находит применение в составе таких сплавов как латунь(сплав цинка и меди) или бронза(сплав олова и меди).
Благодаря высокой электропроводности и устойчивости к коррозии она находит широкое применение в электронике. Из меди изготавливаются электрокабели, различные электрические провода, телефонные линии и микроволновые оболочки. Так же можно отметить сторительную отрасль. В этой отрасли изготавливаются медные плиты, а также листы для кровли. Кроме этого не стоит забывать про декоративную составляющую. В пример можно поставить фурнитуру для мебели и декоративные изделия ручного производства.
Если брать электронику, то медь является составным компонентом различного рода процессоров, аккумуляторов, печатных плат и др. Так же благодаря своей теплопроводности она используется в радиаторах охлаждения. В пример можно поставить радиаторы охлаждения видеокарт и процессоров.
Медь в прямом или косвенном смысле применяется почти во всех областях применения. Будь то пищевые добавки или компонент краски для стекла и керамики. Так же боеприпасы для оружия или краситель для фейрверков(синий цвет). Некоторые медицинские препараты для людей или удобрение для почвы и растений. Медь так же применяется как компонент пожаротушения класса D и для изготовления антимикробных защитных тканей.
Подведя итоги стоит отметить, что на сегодняшний день нет такой отрасли производства где прямого или косвенного участия не принимала бы медь.
Интересные факты
Так как применение меди очень широкое, соответственно и интересных фактов связанных с медью достаточно. Стоит начать с того, что цена на чистую медь на мировом рынке не такая уж и маленькая. В 2014 году 1 тонна меди на мировом рынке оценивалась в 7000 американских долларов. В связи с такой высокой ценой увеличилось количество краж медных предметов. Например в Германии железнодорожная кампания Deutsche Bahn AG понесла убытков на 14 миллионов евро из-за воровства медных заземляющих железнодорожных кабелей.
Еще одним интересным моментом является то, что первые изобретенные человеком зеркала изготавливались именно из меди. Медь натиралась(полировалась) до такой степени, пока не было видно отбражение на поверхности меди. Так же в области применения стоит отметить, что большая часть монет произведенных по всему миру содержит в своем составе медь. Еще одним интересным фактом является то, что медь как железо и алюминий могут подвергаться вторичной переработке без потери своих свойств.
Так же можно отметить и биологическую составляющую меди. В больших количествах она является токсичной, а в малых — неотъемлемая часть существования организма человека. В различных состояниях в человеческом организме содержится около 150 мг меди. Суточная доза потребления меди является нормальной для человека весом 75 кг равной 2 мг.
Таблица Менделеева для чайников
Медь встречается в природе как в соединениях, так и в самородном виде. Промышленное значение имеют халькопирит CuFeS2, также известный как медный колчедан, халькозин Cu2S и борнит Cu5FeS4. Вместе с ними встречаются и другие минералы меди: ковеллин CuS, куприт Cu2O, азурит Cu3(CO3)2(OH)2, малахит Cu2CO3(OH)2. Иногда медь встречается в самородном виде. Самый большой самородок был найден в Северной Америке, а его вес составлял 420 тонн [2]. Сульфиды меди образуются в основном в среднетемпературных гидротермальных жилах. Также нередко встречаются месторождения меди в осадочных породах — медистые песчаники и сланцы. Наиболее известные из месторождений такого типа — Удокан в Читинской области, Джезказган в Казахстане, меденосный пояс Центральной Африки и Мансфельд в Германии.
Большая часть медной руды добывается открытым способом. Содержание меди в руде составляет от 0,4 до 1,0 %.
Видео
Степень окисления меди
Атомы меди в соединениях имеют степени окисления 4, 3, 2, 1, 0.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
История
Медь – один из первых металлов, с которыми имело дело человечество. Этому способствовали преимущества: большая распространенность, доступность, относительно низкая температура плавления.
Достоинства меди люди оценили восемь тысячелетий назад.
Медный век начался сразу после каменного:
- Древнейшими признаны медные артефакты, откопанные на территории современной Турции. Это бусинки и декоративные накладки.
- Из металла делали режущий инструментарий и посуду.
- История открытия медных рудников на Руси начинается на Урале за две тысячи лет до новой эры. Затем были Кавказ, Алтай, Сибирь.
- Промышленная переработка с использованием бронзы началась в XIV веке. Из сплава отливали пушки и колокола.
Из бронзы отлиты Царь-колокол и Царь-пушка.
Предполагается, что металл назван по имени острова Кипр. Здесь еще в III веке до нашей эры обнаружились медные залежи, а население освоило выплавку меди.
Происхождение русскоязычного термина медь «Этимологический словарь русского языка» М.Фасмера увязывает с древненемецким корнем smid – кузнец, металл.
Производство, добыча и запасы меди
Мировая добыча меди в 2000 году составляла около 15 млн т., a в 2004 году — около 14 млн т. [2] [3] . Мировые запасы в 2000 году составляли, по оценке экспертов, 954 млн т., из них 687 млн т. подтверждённые запасы [2] , на долю России приходилось 3.2 % общих и 3.1 % подтверждённых мировых запасов [2] . Таким образом, при нынешних темпах потребления запасов меди хватит примерно на 60 лет.
Производство рафинированной меди в России в 2006 году составило 1,009 тыс. тонн, потребление — 714 тыс. тонн [4] . Основными производителями меди в России являются:
| Компания | тыс. тонн | % |
|---|---|---|
| Норильский никель | 425 | 45 % |
| Уралэлектромедь | 351 | 37 % |
| Русская медная компания | 166 | 18 % |
Как добывают медь Этот металл встречается в природе в самородном виде чаще, чем золото, серебро и железо. Нашли однажды самородок, который весил 420 т. Наверняка медь была первым металлом, с которым познакомились древние люди. Первые свои орудия делали они из кремниевой и железной руды, из меди, и уже потом научились изготовлять их из бронзы и железа. Сплав меди с оловом (бронзу) получили впервые за 3000 лет до н.э. на Ближнем Востоке. Бронза привлекала людей прочностью и хорошей ковкостью, что делало ее пригодной для изготовления орудий труда и охоты, посуды, украшений. Все эти предметы находят в археологических раскопах. Добычу меди называют прабабушкой металлургии. Ее добыча и выплавка были налажены еще в Древнем Египте, во времена фараона Рамзеса II (1300—1200 гг. до н.э.). Древние египтяне нагнетали воздух в плавильные печи с помощью мехов, а древесный уголь получали из акации и финиковой пальмы. Они выплавили около 100 т чистой меди. На территории России и сопредельных стран медные рудники появились за два тысячелетия до н.э. Остатки их находят на Урале, в Закавказье, на Украине, в Сибири, на Алтае. В XIII—XIV вв. освоили промышленную выплавку меди. В Москве в XV в. был основан Пушечный двор, где отливали из бронзы орудия разных калибров. О нем напоминает теперешняя Пушечная улица в Москве. Сейчас известно более 170 минералов, содержащих медь, но из них только 14—15 имеют промышленное значение. Это — халькопирит (он же медный колчедан), малахит, встречается и самородная медь. В медных рудах часто в качестве примесей встречаются молибден, никель, свинец, кобальт, реже — золото, серебро. Обычно мед-ные руды обогащаются на фабриках, прежде чем поступают на медеплавильные комбинаты. Богаты медью Казахстан, США, Чили, Канада, африканские страны — Заир, Замбия, Южно-Африканская республика. Очень крупное Удоканское месторождение медной руды сравнительно недавно обнаружено на севере Читинской области.
Большая часть добываемой меди используется в электротехнике, потому что медь обладает высокой электропроводностью, уступая в этом только серебру, которое, конечно, намного дороже. Миллионы километров проводов опутали земной шар, и большинство из них медные. Медь нужна для производства двигателей, телевизоров, телефонных аппаратов, различных электроприборов, автомобилей, электровозов, холодильников и даже музыкальных инструментов. Ее используют в химической промышленности для борьбы с вредителями садов и огородов, для подкормки растений и животных. Всюду нужна медь. По объему мирового производства и потребления медь занимает третье место после железа и алюминия.
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Физические свойства
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности после серебра). Имеет два стабильных изотопа — 63 Cu и 65 Cu, и несколько радиоактивных изотопов. Самый долгоживущий из них, 64 Cu, имеет период полураспада 12,7 ч и два различных варианта распада с различными продуктами.
Плотность — 8,94*10³ кг/м³
Удельная теплоёмкость при 20 °С — 390 Дж/кг*К
Удельное электрическое сопротивление при 20-100 °С — 1,78·10 -8 Ом·м
Существует ряд сплавов меди: латунь — сплав меди с цинком, бронза — сплав меди с оловом, мельхиор — сплав меди и никеля, и некоторые другие.
Мировая цена меди устанавливается на Лондонской бирже металлов. Она зависит от спроса, определяемого состоянием экономики.
И колеблется соответственно:
- К началу 2008 года преодолена психологическая отметка $8000 за тонну.
- Через полгода было уже $+940, что стало рекордом за всю историю биржи.
- На начало 2011 года взята планка $10 000.
Затем произошел спад. На 2021 год тонна меди торгуется по $8057. Сказалось торможение экономики из-за пандемии коронавируса.
Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов
Переходные элементы имеют d- и f-электроны, у них происходит заполнение внутренних оболочек. В Периодической системе химических элементов (ПСХЭ) они заполняют В-группы (побочные) 4, 5 и 6 периодов (рис. 1). В основном расположены между s- и р-элементами.
Рис. 1. Периодическая таблица
Наибольшее практическое значение среди переходных элементов имеют медь, цинк, хром и железо. На примере элементов, простых веществ и соединений можно проследить общие закономерности изменения свойств.
Медь, Cu
Латинское название — Cuprum, символ — Cu. Относительная атомная масса — 63,5. Медь находится в 4 периоде, I B-группе ПСХЭ. Порядковый номер — 29.
Распределение электронов по уровням и подуровням характеризует следующая электронная формула: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 . В возбужденном состоянии на 4s уровень и подуровень «проскакивает» один d-электрон. Атом получает более устойчивую конфигурацию электронных оболочек.
Типичные значения валентностей и степеней окисления в соединениях: I(+), II(+), 0, +1, +2 соответственно. Заряд катиона 2+.
Способ получения меди в лаборатории — восстановление из оксида с помощью водорода при нагревании.
- Восстановление водородом. Схема процесса: Cu +2 O + H2 → Cu 0 + H2O.
- Металлотермия. Происходит реакция обмена CuO + H2SO4 → CuSO4 + H2O. далее идет вытеснение меди железом CuSO4 + Fe → FeSO4 + Cu↓.
- Электролиз водного раствора сульфата меди. На катоде происходит восстановление Cu 2+ + 2ē → Cu 0 ; на аноде — окисление 2H2O – 4ē → 4H + + O2↑.
Описание металла — простого вещества
- золотисто-красный цвет (рис. 2);
- металлический блеск;
- пластичен, легко вытягивается в проволоку и прокатывается в листы;
- тепло- и электропроводность высокие.
Рис. 2. Медь
Химические свойства:
- Медь в ряду активности находится после водорода, это инертный металл.
- Не взаимодействует с водой.
- Не реагирует при обычных условиях с водородом, углеродом, кремнием, азотом, с растворами соляной и серной кислот, растворами щелочей.
- Взаимодействует с концентрированными растворами серной и азотной кислот.
Важнейшие соединения меди
Класс веществ
Название соединения
Характер свойств
Оксид меди (II) CuO
Амфотерный (преобладают основные свойства).
Гидроксид меди (I) СuOH
Применение меди, ее соединений и сплавов:
- изготовление конденсаторов, механизмов для часов, ювелирных изделий с применением латуни (сплава);
- использование чистого металла и сплавов в машиностроении;
- использование оксидов в производстве стекла, эмалей;
- производство дистилляторов воды;
- выпуск проволоки, кабеля.
Кристаллогидрат сульфата меди (медный купорос) — средство для борьбы с грибковыми инфекциями растений. Применяется в смеси с гашеной известью для получения более сильной бордоской жидкости. Медь используется в производстве микроудобрений. Элемент необходим растениям и животным для нормального роста и развития.
Цинк, Zn
Латинское название Zincum, химический символ Zn. Элемент 4 периода, расположен во II группе, В-подгруппе. Порядковый номер 30. Масса — 65,37. Строение электронных оболочек: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 (в основном состоянии). Валентность и степень окисления: II(+) и +2 (соответственно).
Способы получения в промышленности:
- Восстановление углеродом при нагревании: ZnO+ C → CO↑ + Zn.
- Гидрометаллургия: ZnO + H2SO4 → ZnSO4+ H2O; ZnSO4+ Fe → FeSO4+ Zn↓.
- Электролиз: цинк восстанавливается на катоде Zn 2+ + 2H + + 4ē → Zn↓ + H2.
Цинк — металл серебристо-серого цвета (рис. 3). Твердый, проводит тепло и электричество. Окисляется кислородом при нагревании. Не взаимодействует с бором, углеродом, кремнием, азотом. В воде не растворяется, но при сильном нагревании реагирует с водяным паром с образованием оксида цинка и выделением водорода. Реагирует с кислотами, кроме азотной, вытесняет водород. Вытесняет металлы, расположенные в ряду активности правее, из растворов их солей.
Рис. 3. Цинк
Характеристика соединений
Классы веществ
Названия и формулы
Свойства
Оксид цинка, ZnO
Гидроксид цинка Zn(ОН)2
Цинк находит применение как защитный материал для предотвращения ржавчины (оцинковки) изделий из стали, железа. Металл используется в строительстве, производстве бытовой техники и для других целей.
Хром, Cr
Латинское название Chromium, химический символ Cr. Элемент 4 периода, VI В-группы. Порядковый номер 24. Относительная атомная масса — 52. Строение электронных оболочек характеризует формула 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1 (в невозбужденном состоянии).
Значения валентности и степени окисления в соединениях: II(+), III(+) VI(+); +2, +3, +6 (соответственно). Наиболее устойчивое состояние достигается при степени окисления +3. Повышение значения ведет к появлению и возрастанию кислотных свойств, ослаблению основных.
Способы получения в промышленности — пирометаллургия и электролиз. В первом случае используется вытеснение алюминием из оксида. Схема процесса: Cr2O3 + 2Al → Al2O3 + 2Cr. Проводят электролиз концентрированных водных растворов оксидов (CrO3 или Cr2O3), либо соли Cr2(SO4)3. Второй метод служит для получения наиболее чистого вещества.
Хром — твердый металл серого цвета с металлическим блеском (рис. 4). Вытесняет водород при взаимодействии с растворами неокисляющих кислот (соляной, фосфорной и др.). При сильном нагревании растворяется в серной и азотной кислотах.
Рис. 4. Хром
Химические свойства соединений
Классы веществ
Названия и формулы
Свойства
Гидроксид хрома (II), Сг(ОН)2.
Металл применяется для хромирования стали, изготовления декоративных изделий, бижутерии. Растворами солей пропитывают древесину для защиты от вредителей. Хром применяется для изготовления красителей, окраски стекла.
Железо, Fe
Латинское название Ferrum, химический символ Fe. Элемент находится в 4 периоде, VIII В-группе ПСХЭ. Порядковый номер 26. Относительная атомная масса — 56. Строение электронных оболочек характеризует формула 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2 (в невозбужденном состоянии).
Значения валентности и степени окисления в соединениях: II(+), III(+) VI(+); +2, +3, +6 (соответственно). Самое устойчивое состояние — при степени окисления +3. Железо в степени окисления +6 — сильный окислитель.
Железо получают в промышленности двумя основными способами. Пирометаллургический заключается в восстановлении алюминием или водородом при высоких температурах. Схема алюмотермии: Fe3O4 + 4H2 → 3Fe + 4H2O. Подвергают растворы солей, например хлорид. На катоде происходит восстановление по схеме: Fe +3 + 3ē → Fe↓. На аноде собирают газообразный хлор. Сплавы железа — чугун и сталь — производят в мартеновских печах, получают электрометаллургическим способом.
Железо — твердый металл серебристо-черного цвета с металлическим блеском (рис. 5). Взаимодействует с кислородом при сильном нагревании. Вытесняет водород из растворов кислот. В воде окисляется с образованием оксидов и гидроксидов. Эту смесь в быту называют ржавчиной (рис. 6).





.png)